Фазовый состав и его влияние на коррозионную стойкость исследовали ученые лаборатории жаропрочных сплавов на основе никеля и железа Уральского федерального университета под руководством Аркадия Жилакова, кандидата наук по материаловедению.

Почему ржавеет медь и как защитить ее от коррозии
Изделия из меди используются человеком уже несколько веков. В дореволюционные времена цена этого металла была равна цене золота, настолько дорого стоило его производство. Сегодня медь намного дешевле, поэтому из нее также изготавливают ювелирные изделия, посуду, аксессуары для интерьера и другие предметы.

Коррозия меди, в отличие от железа, развивается медленно благодаря ее устойчивости к этому явлению, но иногда приходится принимать меры, чтобы очистить изделия от неприглядного потускнения.
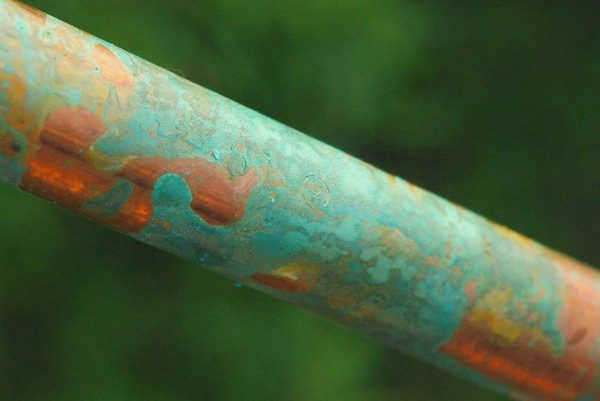
Что такое коррозия металлов и сплавов
Коррозия – это процесс разрушения металла под воздействием агрессивных факторов окружающей среды. Все металлы и сплавы корродируют в большей или меньшей степени, вызывая ржавчину и участки разрушения (дыры). Неметаллические металлы также могут разрушаться со временем: примером может служить старение резины или пластика из-за взаимодействия с кислородом, частого контакта с водой и перепадов температуры.
Основной причиной коррозии считается термодинамическая нестабильность металла под воздействием физических агентов или химических веществ, присутствующих в контактной среде. По сравнению с железом, медь окисляется с гораздо меньшей скоростью, но при повышении температуры процесс значительно ускоряется. При регулярном воздействии температуры выше +100 градусов любой металл ржавеет в несколько раз быстрее.
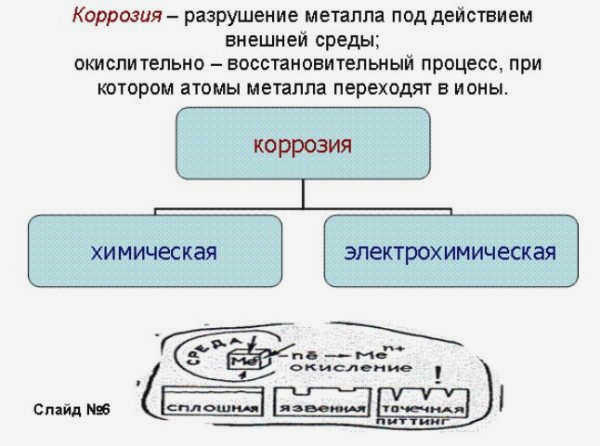
Коррозия металлов/сплавов – что это такое?
Ржавление – это процесс разрушения металла под воздействием негативных факторов окружающей среды. Все металлы и сплавы в той или иной степени ржавеют, что приводит к появлению ржавчины и участков нарушения целостности (например, дыр). Со временем все неметаллы могут начать разрушаться – в качестве примера можно привести старение резины или даже пластика из-за воздействия кислорода, постоянного контакта с водой и перепадов температуры.
Основной причиной ржавления можно считать термодинамическую неустойчивость металла к воздействию физических или даже химических факторов, присутствующих в контактной среде. По сравнению с железом, медь окисляется в гораздо меньшей степени, но этот процесс значительно ускоряется при повышении температуры. При регулярном воздействии среды выше +105 градусов любой металл ржавеет в несколько раз быстрее.
Для получения дополнительной информации см.
Коррозионные свойства
Медь – очень ковкий металл красновато-золотистого цвета, а после удаления оксидного слоя – слегка розоватого. По электропроводности она уступает только серебру, а также имеет высокую степень теплопроводности. Благодаря низкому удельному сопротивлению медь используется в электротехнике – из нее изготавливают медные пластины, обмотки электродвигателей и провода.
Следует отметить, что благодаря своим отличным антикоррозионным свойствам этот металл включают в состав сплавов для улучшения их инженерных свойств (латунь, бронза и другие). В гальванической среде медь становится катодом и начинает участвовать в электрохимических процессах, вызывая ускоренное ржавление других металлов.
Медь является неактивным химическим элементом и поэтому практически не взаимодействует с водой (морской или пресной). Если воздух сухой, на поверхности материала образуется оксидный слой толщиной до 50 мм. Медное изделие начнет темнеть, приобретая зеленоватый или коричневый цвет, что называется патиной. Во многих случаях патина рассматривается как декоративное покрытие. При контакте с разбавленной соляной кислотой интенсивность коррозии невелика, но при реакции со многими другими кислотами, с галогенами, с "акварегией" металл будет окисляться, образуя карбонат меди.
Условия для разрушения меди
Несмотря на свою устойчивость к разрушению, даже медные изделия могут ржаветь при определенных условиях. Эти явления менее выражены в воде, влажном воздухе, почве и тем более в кислой среде. Коррозию можно значительно уменьшить с помощью оловянирования – покрытия меди слоем олова. Высококачественное оловянирование обеспечивает надежность и защиту от дефектов, а также повышает коррозионную стойкость, делая материал устойчивым к воздействию жары, града, дождя и снега. Изделия с оловянным покрытием прослужат более века, не теряя своих первоначальных свойств.
Что такое коррозия
Коррозия – это разрушение металла в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой. Науке известно множество видов коррозии, и все они начинаются по-разному.
Самой простой формой коррозии является химическое окисление. Воздух содержит 21 процент кислорода, который является сильным окислителем и всегда готов вступить в реакцию с металлами, превращая их в соответствующие оксиды. Чтобы оценить основную способность и скорость этого процесса, необходимо учитывать активность данного металла, давление кислорода и температуру.
Наиболее реакционноспособные щелочные металлы, литий, натрий и другие, немедленно вступают в бурную реакцию с кислородом, поэтому в лабораториях их хранят под слоем парафина. Драгоценные металлы, такие как золото и платина, не окисляются даже при самых высоких температурах. Платиновые тигли можно использовать для термогравиметрического анализа при температуре до 1 600 градусов Цельсия.
Другие металлы находятся где-то между этими крайностями. Например, железо (Fe) начинает активно реагировать с кислородом при температуре выше 200 градусов Цельсия, а без нагревания реакция протекает медленно. Оксидный слой, появляющийся на поверхности металла, еще больше замедляет ее: новым молекулам кислорода труднее добраться до поверхности металла. Поэтому конструкции из железа и близкородственных металлов достаточно хорошо ведут себя в сухом воздухе.
Однако все меняется, когда в дело вступает вода.
Просто добавьте воду
Металлические конструкции обычно содержат детали из другого металла или сплава, например, заклепки и соединения. При погружении в воду точка контакта между двумя металлами действует как гальванический элемент, т.е. химический источник электрического тока. Для этого не нужны провода – проводником служит вся металлическая конструкция. Более активный металл (с более низким потенциалом восстановления электрода) становится "анодом": он передает часть своей электронной плотности другому металлу, а сам металл начинает растворяться, переходя в катионное состояние. Менее активный металл действует как "катод": электроны, полученные на нем, используются для восстановления кислорода.
Два новых иона, катион металла и кислородсодержащий анион, соединяются, образуя гидроксид или оксид. Другой металл обычно не участвует в химических реакциях и остается лишь проводником электронов. Образовавшийся оксид находится в твердом контакте с жидкостью. Вода с растворенным кислородом может проникнуть под оксидный слой и взаимодействовать с ним, и тогда реакция будет продолжаться. Именно это произошло в случае с обшивкой фрегата "Алерт": катодом была медь, а анодом – железные гвозди.
Нежелательный гальванический компонент может образоваться и на однородной металлической структуре – вблизи дефекта, шероховатости или примеси. Все такие процессы относятся к электрохимической коррозии коррозия.
Если металл взаимодействует с растворами кислот, коррозия происходит еще быстрее. При этом различные металлы не обязательно должны находиться рядом друг с другом: металл может вступать в окислительно-восстановительную реакцию с катионами водорода H+ , образуя соль соответствующей кислоты и атомарный водород.
Коррозию металлов также ускоряют солевые растворы. Во-первых, чем выше их концентрация, тем выше проводимость и тем быстрее движутся ионы. Кроме того, например, высокое содержание хлоридов (солей соляной кислоты) вызывает специфический процесс – хлоридную коррозию. Хлорид-ионы осаждаются в формирующемся слое ржавчины и увеличивают его проницаемость. В результате скорость коррозии увеличивается.
Условия для разрушения материалов
Несмотря на устойчивость к коррозии, даже медные изделия могут ржаветь при определенных условиях. Такие явления менее выражены во влажном воздухе, воде и почве и более выражены в кислой среде.
Серьезным способом снижения коррозии является лужение – покрытие меди слоем олова. Качественное лужение обеспечивает надежную защиту от повреждений, повышает коррозионную стойкость и делает материал устойчивым к воздействию высоких температур, дождя, града и снега. Срок службы изделий, покрытых оловом, составляет более 100 лет без потери первоначальных свойств.

Влияние воды
Скорость коррозии меди в воде сильно зависит от наличия оксидного слоя на ее поверхности, а также от насыщенности воды кислородом. Чем выше содержание кислорода в воде, тем сильнее разрушение материала. В целом, медь считается устойчивой к разрушительному воздействию соленой и пресной воды, и только растворенные ионы хлора и низкий уровень pH оказывают на нее пагубное влияние. Долговечность и устойчивость к ржавчине позволяют использовать этот материал для трубопроводов.
Если на поверхности изделия с медным покрытием имеется коричневый или зеленый оксидный слой, то проникновение разрушающих веществ невелико. Оксидный слой обычно образуется после 60 дней пребывания в воде. Зеленая (карбонатная) корка считается более прочной, а черная (сульфатная) – хрупкой и менее прочной.
В морской воде уровень коррозии почти такой же, как и в пресной. Только при ускорении движения жидкости коррозия становится ударной и, следовательно, более интенсивной. Медь – материал, неспособный к загрязнению морскими микроорганизмами, поскольку ее ионы губительны для ракообразных и водорослей. Это свойство металла используется в судоходстве и рыболовстве.

Коррозия меди в почве
Коррозия меди в почве сильно зависит от значения pH почвы. Чем более щелочная или кислая почва, тем быстрее медь корродирует в почве. Аэрация и влажность почвы оказывают меньшее влияние. Коррозия меди и ее сплавов усиливается, если почва сильно насыщена микроорганизмами. Это объясняется тем, что некоторые из них в процессе своей жизнедеятельности выделяют сероводород, который разрушает защитный оксидный слой.
Продукты почвенной коррозии меди и ее сплавов имеют более сложный состав, чем продукты атмосферной коррозии, и обладают слоистой структурой.
Если медный предмет пролежал в земле очень долго, он может полностью превратиться в рыхлую, светло-зеленую массу, состоящую из продуктов коррозии меди. Если предмет пролежал в земле недолго, может наблюдаться лишь небольшой слой патины, который легко удаляется механическим путем.
Методы извлечения меди
В природе медь встречается в соединениях и в кусковой форме. Соединения представлены оксидами, углеводородами, сульфидными и карбонатными комплексами, а также сульфидными рудами. Наиболее распространенными рудами являются медный пирит и медная известь. Содержание меди в них составляет 1-2%. 90% первичной меди добывается пирометаллургическими методами и 10% – гидрометаллургическими.
1. Пирометаллургический метод включает следующие процессы: обогащение и обжиг, выплавку штейна, продувку конвертера и электролитическое рафинирование.
Медные руды обогащаются флотацией и окислительным обжигом. Суть метода флотации заключается в следующем: частицы меди, взвешенные в водной среде, прилипают к поверхности пузырьков и всплывают на поверхность. Этот метод позволяет получить порошкообразный медный концентрат, содержащий 10-35% меди.
Окислительный обжиг подходит для медных руд и концентратов со значительным содержанием серы. При нагревании в присутствии кислорода сульфиды окисляются, и количество серы уменьшается почти наполовину. Слабые концентраты с содержанием меди 8-25% подвергаются обжигу. Богатые концентраты с содержанием меди 25-35% выплавляются без обжига.
Следующим этапом пирометаллургического метода производства меди является штейновая плавка. Если в качестве сырья используется кусковая медная руда с высоким содержанием серы, то плавка происходит в шахтных печах. В случае использования порошкообразного флотационного концентрата применяются отражательные печи. Плавка происходит при температуре 1450 °C.
В горизонтальных конвертерах с боковой продувкой медный мат продувается сжатым воздухом для окисления сульфидов и железа. Полученные оксиды затем преобразуются в шлак, а сера – в оксид. Конвертер производит черновую медь, которая содержит 98,4-99,4% меди, железа, серы, а также следы никеля, олова, серебра и золота.
Черновая медь подвергается пламенному и электролитическому рафинированию. Примеси удаляются с помощью газов и превращаются в шлак. Процесс пламенного рафинирования позволяет получить медь чистотой до 99,5%. После электролитического рафинирования чистота составляет 99,95%.
Применение меди
Благодаря своим ценным свойствам медь и медные сплавы используются в электротехнической и электромеханической промышленности, а также в радио- и приборостроении. Сплавы меди выпускаются с такими металлами, как цинк, олово, алюминий, никель, титан, серебро и золото. Реже встречаются сплавы с неметаллами: фосфором, серой и кислородом. Существует две группы медных сплавов: латунь (сплавы с цинком) и бронза (сплавы с другими элементами).
Медь отличается высокой экологичностью, что позволяет использовать ее в строительстве жилых зданий. Например, медная кровля, благодаря своим антикоррозийным свойствам, может прослужить более века без специального ухода и покраски.
Медь, сплавленная с золотом, используется в ювелирных изделиях. Этот сплав увеличивает прочность изделия и повышает его устойчивость к деформации и истиранию.
Соединения меди характеризуются высокой биологической активностью. В растениях медь участвует в синтезе хлорофилла. Поэтому ее можно найти в составе минеральных удобрений. Дефицит меди в организме человека может привести к ухудшению состава крови. Она содержится во многих продуктах питания. Например, металл содержится в молоке. Однако важно помнить, что избыток соединений меди может вызвать отравление. Поэтому не следует готовить пищу в медной посуде. Большое количество меди может попасть в пищу во время приготовления. С другой стороны, если внутренняя поверхность посуды покрыта слоем олова, опасность отравления отсутствует.
В медицине медь используется как антисептик и вяжущее средство. Она входит в состав глазных капель для лечения конъюнктивита и растворов для лечения ожогов.
